
近日, 美国血液学学会(ASH)会议公布了一份最新的研究成果摘要,宾夕法尼亚大学Dr. Milone研究团队,宣布其可在短短24小时内产生功能性CD19特异性CAR-T细胞(CART19),此方法是5天、3天CAR-T制备技术上的又一更新。该研究团队将于12月9日在ASH会议上公布更多的数据。
 ( 图片来源:ash.confex)
( 图片来源:ash.confex)
该研究的通信作者Dr. Michael Milone是宾夕法尼亚大学医院和医学院的病理学和检验医学副教授。他于1999年从新泽西州的医学和牙科大学获得医学博士学位;在宾夕法尼亚大学继续接受内科,实验室医学和输血医学的研究生医学培训;在博士后研究期间继续科学研究;是宾大的Carl June博士CAR-T项目的早起原研人员,这项工作导致了对B细胞白血病和淋巴瘤患者的人工抗原受体的开放式I期研究。
 (图片来源:med.upenn.edu)
Michael Milone, MD, PhD
Associate Professor of Pathology and Laboratory Medicine
(图片来源:med.upenn.edu)
Michael Milone, MD, PhD
Associate Professor of Pathology and Laboratory Medicine
14年前,Dr. Milone与贝赛尔特董事长兼首席科学家许中伟教授是Carl June团队CAR-T项目最早的原研人员,他们研发的CTL-019最终成为了人类第一个被FDA批准的CAR-T药物。许教授在参加“细胞治疗国际研讨会上”提道:“未来,CAR-T细胞制备的工艺极其重要。随着细胞制备的周期不断缩短,“24小时CAR”、甚至“vein-to-vein”CAR-T的产生,除了极大地降低了综合成本,也将颠覆现有的生产模式和概念。”这对于病情进展迅速的患者来说是至关重要的。
 许中伟教授在“2019(第十届)细胞治疗国际研讨会”上提出CAR-T生产“vein-to-vein”模式和概念。
许中伟教授在“2019(第十届)细胞治疗国际研讨会”上提出CAR-T生产“vein-to-vein”模式和概念。
 许中伟教授与Michael Milone在北京大学未名湖畔合影。
许中伟教授与Michael Milone在北京大学未名湖畔合影。
许教授回国后,引荐Dr. Michael Milone成为“北京大学免疫系客座教授”兼“贝赛尔特公司特约顾问”,共同为细胞免疫治疗行业助力
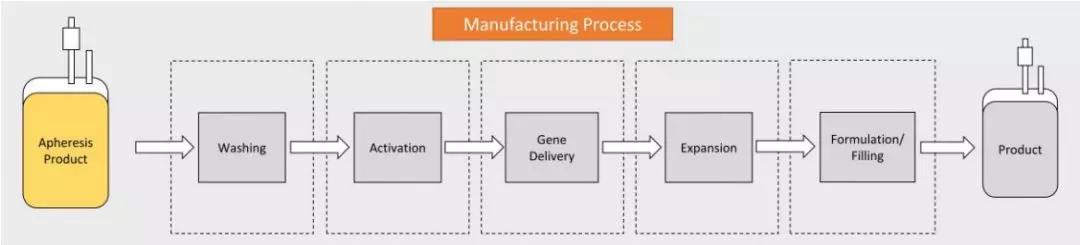 CAR-T细胞制造过程的流程图(图片来源:discovery.ucl.ac.uk)
CAR-T细胞制造过程的流程图(图片来源:discovery.ucl.ac.uk)
在目前的细胞治疗开发过程中,尽管CAR-T细胞的生产通过各种制造方法进行,但所有制造方法都包括相同的共同步骤。
首先,通过白细胞分离术分离患者的白细胞(WBC)并洗涤。然后,激活T细胞,用CAR转基因转导,扩增至所需的细胞数量用于治疗,制剂生产和灌装。在对患者进行质量控制测试和预备性淋巴清除化学疗法后,将产品注射到患者体内。
 (图片来源:discovery.ucl.ac.uk)
(图片来源:discovery.ucl.ac.uk)
白细胞分离术和细胞洗涤 T细胞疗法开始于通过白细胞分离法获得患者的WBC,这是一种将白细胞与全血分离的单采血液成分术。通常采用连续或者半连续的密度梯度离心方法。在分离过程中添加的抗凝剂,红细胞和血小板在洗涤过程中会被清除。抗凝剂在活化的过程中能够改变细胞的特征,红细胞会影响产品的临床效果,血小板会导致细胞的聚集。洗涤后,直接使用WBCs或者WBCs经程序降温冷冻保存。
富集和细胞 一些研究人员使用CliniMACS系统对细胞进行富集和洗涤,其中相应的抗体与顺磁珠连接。FredHutchinson Cancer研究中心和西雅图儿童医院为CD4+(辅助性T细胞)和CD8+细胞(细胞毒T细胞)富集WBC,以便输入具有确定的CD8+/CD4+细胞比例的产品。类似的,Brown等富集收集CD62L+细胞。MDAnderson癌症中心发现NK细胞会阻碍T细胞的培养。当NK细胞超过10%时,使用CD56+磁珠可以去除NK细胞。拉莫斯等人在具有> 95%循环白血病细胞的两名患者中进行CD3 +选择,以使得能够从含有低百分比的T细胞的单采血液成分产物中扩增。
活化 在体内,通过抗原呈递细胞,例如树突细胞(DC)刺激天然T细胞的增殖和分化。T细胞通过T细胞受体(TCR)与位于DC细胞表面的主要组织相容性复合物之间的相互作用以及通过共刺激分子(如CD28,4-1BB和OX40)激活。为了避免与DC共培养繁琐的过程,已经开发并实施了几种模拟T细胞天然刺激的方法。最基本的方法是加入OKT3(抗CD3单克隆抗体)和白细胞介素。
基因递送 基因递送可以分为病毒和非病毒的方法。在CAR-T细胞治疗中,包括电转DNA,转座子系统以及病毒载体,尤其是慢病毒或逆转录病毒转染。病毒转导是最常见的基因递送方法。
扩增 在目前的细胞培养过程中,通常增加培养基体积;通常通过增加袋子或烧瓶的尺寸或通过从板到烧瓶,烧瓶到静态培养袋或静态培养袋换成RM生物反应器。
目前,在所有CAR-T研究机构中,宾夕法尼亚大学接受了大多数的患者;细胞的靶点通常是CD19 ,起源产品主要是自体T细胞;大多数CAR-T细胞产品的制造时间在14天;CAR-T细胞疗法主要用于治疗血液系统恶性肿瘤。
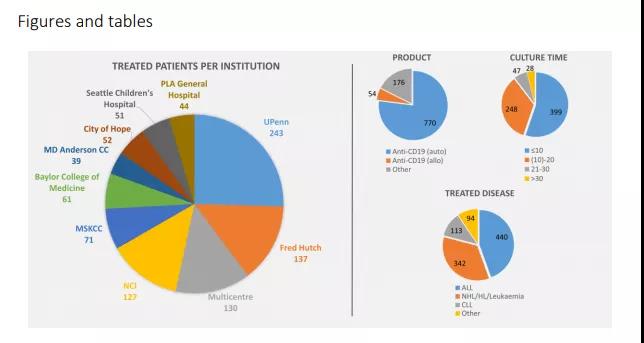 图表分析( 图片来源:discovery.ucl.ac.uk)
图表分析( 图片来源:discovery.ucl.ac.uk)
CAR-T细胞疗法的疗效取决于过继转移后T细胞的植入和持久性。植入和持久性的潜力与T细胞分化的状态有关,宾大团队此前已经证明减少离体培养的持续时间将限制T细胞分化并提高CAR-T细胞疗法的疗效。但是大多数实验方案通常先通过TCR和共刺激受体的结合激活T细胞,然后将T细胞离体扩增9到14天,这对于CAR-T细胞疗法的疗效产生了一定的影响。
于近期发表在ASH年会上的研究摘要,宾大团队描述了使用慢病毒载体可在一天内产生功能性CD19特异性CAR-T细胞(CART19),而无需事先激活T细胞。该摘要显示了使用非优化过程,可以使用表达红外红色荧光蛋白(iRFP)的慢病毒载体转导平均6.5%(范围为2%-10%)的新鲜分离的静态T细胞,与活化的T细胞转导相比,表达动力学更慢(静态和活化T细胞分别在96小时和48小时达到峰值)。尽管与活化的T细胞相比效率低得多,但在所有T细胞亚群中检测,其中央记忆T细胞显示出最大的转导效率;与未处理的T细胞相比,平均转导率高4倍。
宾大团队证明了即使没有逆转录或整合酶功能,CAR表达也可以在静态的T细胞中发生,即所谓的“伪转导”。重要的是,宾大团队证明了该表达产生的CAR-T细胞具有溶细胞活性和效应细胞因子,对抗原的反应类似于激活和转导的CAR-T细胞。
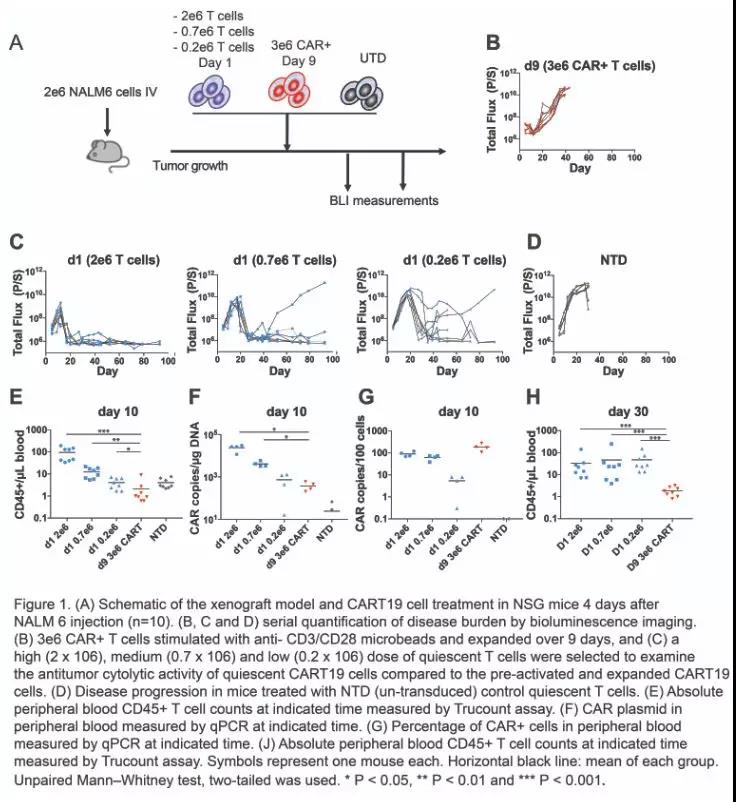 ( 图片来源:ash.confex)
( 图片来源:ash.confex)
该研究团队使用公认的急性淋巴母细胞白血病Nalm6模型进行试验,发现由静态T细胞转导16小时后洗涤去除载体产生的CART19细胞表现出剂量依赖性的抗白血病活性,该活性只要注射小剂量即可持久2x10^5个T细胞。
利用慢病毒载体将基因转移到静态T细胞的能力,描述的高度简化的制造方法具有增强治疗效力的潜力,同时还大大降低了成本。此外,这种制造方法还可能扩大接受疗法的患者数量。
文章来源:
1.https://ash.confex.com/ash/2019/webprogram/Paper131147.html 2.https://discovery.ucl.ac.uk/id/eprint/10050033/1/Veraitch_20180109_CAR%20T%20cell%20manufacturing%20Review%20-%20Revision.pdf 3.https://www.med.upenn.edu/cci/milonelab/